-
화학반응공학 실험 보고서_Al-air battery 예비 보고서_Ver2_200516_R0화학공학실험 족보 2020. 5. 16. 14:00
1. 실험 제목: Al-air Battery
2. 실험 목적
- 배터리의 기본적인 구성과 원리를 이해하고 이를 통해 Al-air battery를 제조 및 이해한다. 전해액의 종류와 농도에 따른 OCV와 방전용량을 계산하여 상관관계를 알아본다.
3. 기본 이론
1) 배터리의 구성 요소, 종류 및 특징
가. 배터리의 구성요소
배터리란, 두 가지의 전극(양극과 음극)을 전해액에 잠기게 하여 각 전극의 활물질과 전해액이 갖는 화학에너지를 전기에너지로 변환시켜 양극과 음극을 연결한 외부회로에서 전기적 에너지를 발생시킬 수 있는 능력을 지닌 것을 일컫는다. 모든 배터리는 양극과 음극을 가지고 있고, 분리 막에 의해 서로 떨어져 있으며 또한 두 전극 사이의 이온 전달을 가능케 하는 전해액에 담겨져 있다.
① Cathode : 외부 도선에서 전자를 받아 환원되는 전극이다. 상대적으로 이온화 경향이 낮은 금속이다.
② Anode: 음극활물질이 산화되어 전자를 방출하는 전극으로 Cathode에 비해 이온화 경향이 높은 금속이다.
③ 전해액(electrolyte): 양이온과 음이온을 가지고 있어 전류가 흐를 수 있도록 하는 물질
④ 분리막(separator): 양극과 음극의 물리적 접촉 방지를 위한 격리막
(활물질 : 전지의 전극에서 전기를 일으키는 반응에 관여하는 물질)
나. 배터리의 종류 및 특징
배터리는 가장 크게 화학 전지와 물리 전지로 나눌 수 있고 화학 전지는 1차 전지, 2차 전지, 연료 전지 등으로 나뉘며, 물리 전지는 태양 전지로 분류된다. 여기서 실생활에서 주로 사용하는 배터리는 주로 1차 전지와 2차 전지다. 전지에 전류를 흘려 전지가 재생되는 과정을 충전이라고 하고, 전지에 있는 에너지를 사용하여 전지가 소모되는 과정을 방전이라고 한다. 1차 전지는 한번 사용하도록 설계된 전지이고, 2차 전지는 충전을 통하여 반복 사용할 수 있도록 설계된 전지이다. 1차 전지로는 수은전지, 산화은전지, 망간전지, 알칼리전지 등이 있고, 2차 전지로는 니켈-카드뮴(Ni-cd)전지, 니켈수소(Ni-CD)전지, 납축전지(Lead_Acid), 리튬 2차전지 등이 있다.
2) Al-air battery의 이론 및 특징
양극과 음극에 각 각 활성탄과 알루미늄 판을 준비하여 anode에서는 OH-(aq)을 받아 금속의 산화반응이 발생하고, cathode에서는 공기 중의 산소와 전해질로부터 생성된 물이 환원 반응을 한다. 이 과정에서 전자가 생성되어 화학적 에너지가 전기적 에너지로 변하게 된다. 다음의 화학식은 Al-air battery에서 양극과 음극의 산화, 환원 반응 그리고 그에 따른 기전력을 나타낸 것이다.
Anode
Al + 3OHㅡ → Al(OH)3+3e-
E = -2.30 V
Cathode
1/2O2 + H2O + 2e- → 2OH-
E = 0.401 V
Overall
Al(s) + 3/2H2O + 3/4O2 → Al(OH)3
E = -2.73 V
알루미늄-공기 배터리는 공기 중의 산소를 이용하므로 미리 산소를 넣지 않아도 되어서 가볍고 다른 극의 금속은 싼 물질들이므로 실용성이 높다. 또 금속을 연료로 사용하기 때문에 수소 연료전지에 비하여 상대적으로 가격이 저렴하며 출력 밀도가 높고, 화학적으로 안전하다는 장점을 갖는다.
3) 용어설명: open circuit voltage, capacity, specific energy density, self-discharge
가. Open circuit voltage
Open circuit voltage란 전지에 부하를 걸지 않은 상태에서의 양 단자 간 전압을 말한다. 즉, 전지를 기기에 접속하지 않은 상태(전류를 흘리지 않은 상태)에서의 전지 양 단자 간 전압이다. 실제로는 흐르는 전류에 의하여 전지의 내부저항에 상당하는 전압강하가 생기며 그것을 개회로 전압에서 빼 낸 만큼의 낮은 전압이 전지단자에 나타나게 된다.
나. Capacity
Capacity란 전지를 기기에 사용했을 때 기기를 사용할 수 없게 될 때까지 나오는 전하량을 말한다. Capacity(전지 용량)의 단위는 패럿(F)이며, 1F는 1V의 전압을 걸어 주었을 때 1C의 전하가 충전되는 전기 용량이다. Capacity의 전하량은 다음과 같은 식으로 표현 할 수 있다.
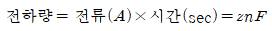
(F : Faraday constant, 96500C/mol, 전하량 : C(쿨롱), 1C= 1A 1Sec)
다. Specific energy density
Specific energy density란, 전지에서 나올 수 있는 에너지의 양을 단위 질량 당 값으로 나타낸 것이다. 질량 에너지 밀도라고도 한다. 질량 에너지 밀도가 큰 전지일수록, 가벼운 전지를 만드는 것이 즉, 경량화가 가능하다. 전지에서 나올 수 있는 에너지의 양은 전지의 용량과 평균 전압의 곱으로 나타낼 수 있다. 따라서 단위는 Wh/kg 이다.
라. Self-discharge
전지에 부하를 걸지 않은 상태에서 방치(저장)했을 때, 전지 내부의 화학반응에 의해 전지 본래의 사용 가능 용량이 감소되는 현상을 말한다. 일반적으로, 기온이 10℃ 상승할 때마다 방전량은 배가 되며, 장기간 방치하면 축전지의 수명은 짧아진다. Self-discharge의 원인은 전해액 중 불순물에 의해 국부 전지가 형성되거나 극판의 작용 물질의 탈락에 의한 단락, 파손 또는 음극판의 작용물질이 황산과의 화학 작용으로 누설 전류가 흐르기 때문이다. 이로 인하여, 전지의 용량이 줄어들 뿐만 아니라, 누액(전지 내부에서 전해액이 새어 나오는 현상), 내압상승, 변형 등의 전지의 손상을 가져올 수 있기 때문에 주의해야 한다.
4. 실험 방법
1) 알루미늄 호일(15mm * 15mm)을 준비한다.
2) KOH, NaCl, H3Po4를 0.5M, 1M, 3M로 각각 제조한다.
3) 전해질을 교반시킨다.
4) 알루미늄 호일위에 분리막 역할을 하는 키친 타올을 올리고 활성탄을 첨가한다.
(활성탄을 올리기 전, 방전 용량 계산을 위해 활성탄의 무게를 측정한다.)
5) 활성탄 위에 교반시킨 전해질을 스포이트를 이용해 뿌린다.
6) 그 위에 전선을 올리고 한쪽은 밀봉하고 한쪽은 산소 유입을 위해 개봉한다.
7) 멀티미터로 각 셀의 전압을 측정하고 기록한다.
8) 오토랩으로 일정전류로 방전시켜서 IV curve를 얻고, 면적 당 방전 용량을 계산하도록 한다.
5. 참고문헌
백운기,박문수 전기화학 청문각 2012년 293-296p
오승모 전기화학 자유아카데미 2014년 1장
실용전기화학 효성출판사 2000년 20-22p
금속-공기 전지에서 아연, 알루미늄 소재의 전기화학적 특성연구 한국자원연구소 1993년 5-20p
'화학공학실험 족보' 카테고리의 다른 글
화학반응공학 실험 보고서_전기변색소자(electrochromic) 예비 보고서_Ver2_200516_R0 (0) 2020.05.16 화학반응공학 실험 보고서_Al-air battery 결과 보고서_Ver2_200516_R0 (0) 2020.05.16 화학반응공학 실험 보고서_패터닝 결과 보고서_Ver 2_200421_R0 (1) 2020.04.21 화학반응공학 실험 보고서_패터닝 예비 보고서_Ver 2_200412_R0 (0) 2020.04.21 화학반응공학 실험 보고서_나일론 합성 결과 보고서 2 ver._200421_R0 (0) 2020.04.21